Через раствор соли с концентрацией ионов металла [Mеn+] (моль/дм три) пропускают постоянный ток силой один А в течение одного ч. Используя данные
- Химия
Условие:
Через раствор соли с концентрацией ионов металла [Mеn+] (моль/дм3) пропускают постоянный ток силой 1 А в течение1 ч.
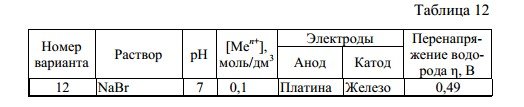
Используя данные табл. 12, выполните следующие задания:
1. Составьте схему электролиза раствора, напишите уравнения процессов, протекающих на электродах. Катодный процесс подтвердите расчетом.
2. Рассчитайте массы(для газов– объем при нормальных условиях) веществ, выделившихся на электродах.
Парциальное давление водорода в воздухе примите равным 5·10–7 атм.
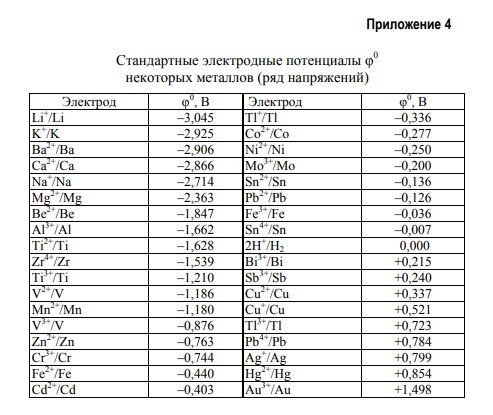
Значения стандартных электродных потенциалов металлов приведены в прил. 4.
Решение:
NaBr = Na+ + Br-
Катодный процесс. При пропускании тока к катоду притягиваются ионы Na+ и диполи H2O.
Рассчитаем значения потенциалов возможных процессов. Величину потенциала металла при прохождении тока i вычисляем по уравнению Нернста без учета поляризации:
(Na+/Na) = 0(Na+/Na) + (0,059 / 1) lg[Na+]
(Na+/Na) = -2,714 В + (0,059 / 1) lg0,1 = -2,773В
Величину равновесного потенциала водорода рассчитывают по уравнению:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства