Дайте термодинамическую характеристику реакции (варианты задания приведены в табл. 4.1) на основании количественных расчётов D0Hr , DS0r , D0Gr .
- Химия
Условие:
Дайте термодинамическую характеристику реакции на основании количественных расчётов 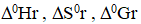 .
.
1. Выпишите из справочных таблиц стандартные термодинамические свойства 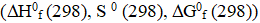 всех веществ, участвующих в реакции.
всех веществ, участвующих в реакции.
2. Охарактеризуйте процесс по величине стандартной энтальпии химической реакции 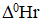 :
:
− рассчитайте стандартную энтальпию химической реакции 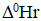
− определите, является реакция экзо- или эндотермической, выделяется или поглощается теплота в результате протекания реакции.
3. Охарактеризуйте процесс по величине стандартной энтропии химической реакции 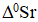 :
:
− рассчитайте стандартную энтропию химической реакции 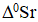 по абсолютным стандартным энтропиям веществ S0 (298);
по абсолютным стандартным энтропиям веществ S0 (298);
− объясните изменение энтропии 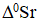 (< 0; > 0; = 0), проведя анализ агрегатного состояния всех участвующих в реакции веществ и сравнив число газообразных молекул исходных веществ и продуктов реакции.
(< 0; > 0; = 0), проведя анализ агрегатного состояния всех участвующих в реакции веществ и сравнив число газообразных молекул исходных веществ и продуктов реакции.
4. Охарактеризуйте процесс по величине энергии Гиббса химической реакции 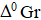 :
:
− Рассчитайте стандартную энергию Гиббса 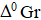 :
:
а) по стандартным энергиям Гиббса образования веществ Δ0Gf (298);
б) по уравнению Гиббса. Сравните полученные величины. Укажите направление протекания реакции при 298 К.
− Определите знаки энергии Гиббса химической реакции 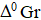 и направление протекания реакции (прямая или обратная) при низких ( T
и направление протекания реакции (прямая или обратная) при низких ( T 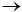 0 ) и при высоких температурах (
0 ) и при высоких температурах ( 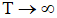 ). Для этого проведите анализ уравнения Гиббса, допуская, что
). Для этого проведите анализ уравнения Гиббса, допуская, что 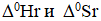 не зависят от температуры.
не зависят от температуры.
5. Сделайте вывод об обратимости процесса. Для обратимой реакции рассчитайте равновесную температуру Тр.
6. Изобразите схематически график зависимости 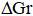 от температуры, используя результаты анализа уравнения Гиббса.
от температуры, используя результаты анализа уравнения Гиббса.
7. Укажите для обратимой реакции, при каких температурах, больших или меньших равновесной Тр, самопроизвольно протекает прямая реакция, а при каких – обратная.
Дано: CaCO3(к) = CaO(к) + CO2(г)
Решение:
Выпишем из справочной таблицы стандартные термодинамические свойства всех участвующих в реакции веществ: стандартную энтальпию образования 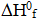 (298), абсолютную стандартную энтропию S0 (298), стандартную энергию Гиббса образования (298) и представим в виде таблицы.
(298), абсолютную стандартную энтропию S0 (298), стандартную энергию Гиббса образования (298) и представим в виде таблицы.
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства