Дано термохимическое уравнение: Fe3O4(тв)+СО(г)=3FeO(тв)+СО2(г), ΔНо298=+34,55 кДж. Используя справочные значения абсолютных стандартных энтропий соответствующих веществ
- Химия
Условие:
Дано термохимическое уравнение: Fe3O4(тв)+СО(г)=3FeO(тв)+СО2(г), ΔНо298=+34,55 кДж. Используя справочные значения абсолютных стандартных энтропий соответствующих веществ (см. прилож., табл. П7), определите, при какой температуре эта система находится в состоянии термодинамического равновесия.
Таблица П7
Стандартные абсолютные энтропии S0 298 некоторых веществ
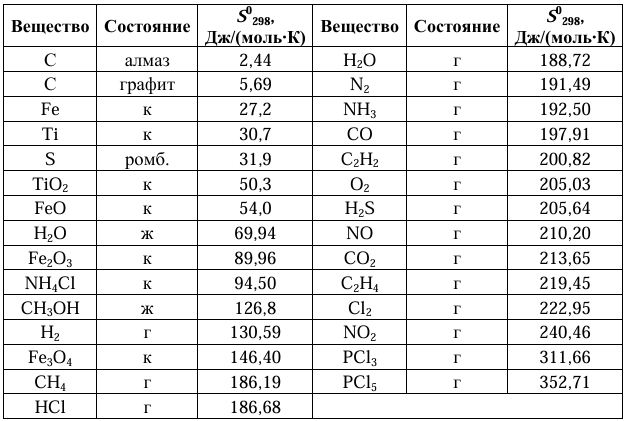
Примечание. Сокращение «ромб.» – указание на конкретную аллотропную модификацию серы (ромбическая); алмаз и графит – соответствующие аллотропные модификации углерода.
Решение:
Находим изменение энтропии системы в ходе протекания химической реакции Fe3O4(тв)+СО(г)=3FeO(тв)+СО2(г):
S0(Fe3O4(тв))=146,40 Дж/(моль∙К)
S0(СО(г))=197,91 Дж/(моль∙К)
S0(FeO(тв))=54,0 Дж/(моль∙К)
S0(СО2(г))=213,65 Дж/(моль∙К)
∆S0...=(3∙S0(FeO)+1∙S(СО)) (1∙S(FeO)+1∙S(СО))=
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства