Условие:
Для растворения 16,8 г двухвалентного металла потребовалось 14,7 г серной кислоты. Определить эквивалентную и атомную (мольную) массы металла и объем выделившегося водорода (н.у.)

Для растворения 16,8 г двухвалентного металла потребовалось 14,7 г серной кислоты. Определить эквивалентную и атомную (мольную) массы металла и объем выделившегося водорода (н.у.)
Определить эквивалентную массу металла мы можем, воспользовавшись законом эквивалентов. Запишем его математическое выражение применительно к данной задаче:
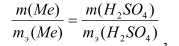
где m(Me) и m(H2SO4) массы металла и кислоты, а mэ(Me) и mэ(H2SO4) - эквивалентные массы металла и кислоты.
2. Эквивалентная масса кислот определяется следующим отношением:
Не нашел нужную задачу?