Для реакции 4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(г) 500, рассчитайте: 1. Тепловой эффект реакции при стандартных условиях (∆Hr0 ,298 ). Выделяется или поглощается тепло при протекании реакции? Эндо- или
- Химия
Условие:
Для реакции, рассчитайте:
1. Тепловой эффект реакции при стандартных условиях (∆Hr0 ,298 ). Выделяется или поглощается тепло при протекании реакции? Эндо- или экзотермической является данная реакция?
2. Изменение энтропии реакции при стандартных условиях (∆Sr0 ,298 ).
3. Изменение энергии Гиббса реакции, протекающей при T1 = 298 К ( ∆Gr0,298 ) и температуре T2 ( ∆Gr0 T2, ), считая, что ∆H0 r и ∆S0 не зависят от температуры. Укажите, какой фактор – энтальпийный или энтропийный – определяет знак ∆Gr0,298 и ∆Gr0 T2, . Сделайте вывод о влиянии температуры на вероятность самопроизвольного протекания процесса в прямом направлении. Все термодинамические расчеты необходимо выполнять с использованием температуры по шкале Кельвина.
реакция: 4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(г) 500
Решение:
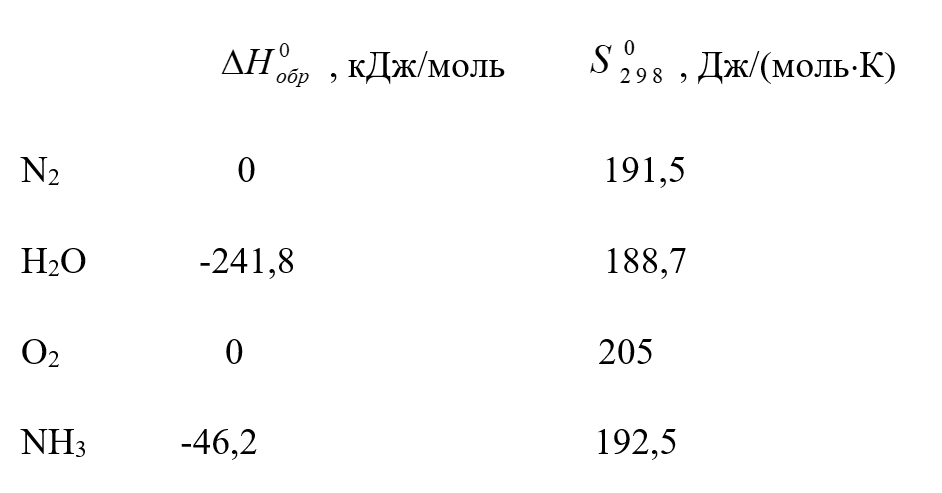
Энтальпийный эффект химической реакции определяют по закону Гесса и следствию из него. Следствие из закона Гесса: изменение энтальпии химической реакции равно разности сумм энтальпий образования продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства