Для реакции синтеза аммиака N2(г) + 3H2(г) = 2NH3(г), = -92,4 кДж 1) Написать математические выражения константы равновесия Кс и Кр и установить взаимосвязь между ними;
«Для реакции синтеза аммиака N2(г) + 3H2(г) = 2NH3(г), = -92,4 кДж 1) Написать математические выражения константы равновесия Кс и Кр и установить взаимосвязь между ними;»
- Химия
Условие:
Для реакции синтеза аммиака N2(г) + 3H2(г) = 2NH3(г), 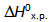 = -92,4 кДж
= -92,4 кДж
1) Написать математические выражения константы равновесия Кс и Кр и установить взаимосвязь между ними;
2) В сторону расходования или образования аммиака сдвигается равновесие при:
а) увеличении давления;
б) увеличении концентрации водорода;
в) введении катализатора.
Решение:
N2(г) + 3H2(г) = 2NH3(г), ![]() = -92,4 кДж
= -92,4 кДж
1) Запишем математическое выражение констант равновесия:
KC = [NH3]2 / [H2]3* [N2]
KP = PNH32 / PH23 * PN2
P равновесные парциальные давления реагентов, указанных в нижнем индексе.
Связь KP и KC устанавливается с использованием закона Клапейрона-Менделеева:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э