Допишите уравнения реакций и составьте к ним электронно-ионные схемы с использованием потенциалов. Для реакций металла с H2SO4(конц) и HNO3 возьмите значение потенциала окислителя, равное 1 В. Оцените устойчивость металлов в данной среде.
- Химия
Условие:
Допишите уравнения реакций и составьте к ним электронно-ионные схемы с использованием потенциалов. Для реакций металла с H2SO4(конц) и HNO3 возьмите значение потенциала окислителя, равное 1 В. Оцените устойчивость металлов в данной среде.
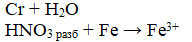
Решение:
1) Восстановителем является Cr.
E (Сr3+/Cr) = 0,74 В;
Вода является окислителем Е(2Н2О/H2) = 0,41 В.
∆E = E (2Н2О/H2) E (Сr3+/Cr) = 0,41 (0,74) = 0,33В 0.
Разность потенциалов окислителя и восстановителя больше нуля, следовательно, реакция возможна (теоретический фактор).
В тонкоизмельченном раскаленном состоянии хром реагирует с водой, образуя гидроксид хрома (III) и водород:
2Cr + 3H2O = 2Cr(OН)3 + 3H2
Реакция протекает при температуре 600-700C (практический фактор). Запишем электронно-ионную схему, ионное и молекулярное уравнения:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства