Используя исходные данные написать уравнения электродных процессов и химической реакции, протекающей в электролизёре. Рассчитать концентрацию электролита, выходящего из ванны регенерации, объём выделившегося на аноде кислорода за один час.
- Химия
Условие:
Скорость циркуляции электролита рафинирования меди через ванну регенерации оставляет 30 л/час. Поступающий в ванну регенерации электролит содержит 90 г/л СuSO4 и 170 г/л H2SO4. Катодный выход по току принять 95%, а анодный 100%. Написать уравнения электродных процессов и химической реакции, протекающей в электролизёре. Рассчитать концентрацию электролита, выходящего из ванны регенерации, объём выделившегося на аноде кислорода за 1 час.
Решение:
На электродах ванн регенерирования электролита протекают следующие электрохимические реакции:
на катоде Сu2+ + 2e = Cu;
на аноде Н2О 2е = 0,5О2 +2Н+;
в ванне Сu2+ +H2O = Cu +0,5O2 + 2H+;
CuSO4 + H2O = Cu +0,5O2 +H2SO4.
Рассчитаем количество меди, выделяющееся на катодах за одну минуту:
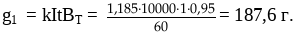
В пересчёте на СuSO4 это составит
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства