Исходя из степени окисления марганца, серы и азота в соединениях КMnО4, Н2S и HNO2, определите, какое из них – окислитель, какое – восстановитель
- Химия
Условие:
Исходя из степени окисления марганца, серы и азота в соединениях КMnО4, Н2S и HNO2, определите, какое из них – окислитель, какое – восстановитель и какое может проявлять как окислительные, так и восстановительные свойства? Почему?
На основании электронных уравнений расставьте коэффициенты, укажите окислитель и восстановитель в уравнениях реакций, идущих по схемам:
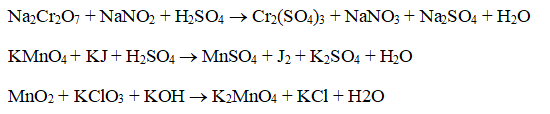
Решение:
Для определения степени окисления атомов элементов в молекуле составляют простейшие алгебраические уравнения
КMnХ О4, х +4( -2) +1 = 0 х = +7
Поскольку +7 это высшая степень окисления для Mn, то
КMnО4, может быть только окислителем
Н2S Х Х + 2( +1) Х = -2
Поскольку -2 это низшая степень окисления для S, то
Н2S может быть только восстановителем
HNХ O2, х +2(-2) +1 = 0 х = +3
Поскольку +3 это промежуточная степень окисления для N , то
HNO2 , может быть как окислителем , так и восстановителем
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства