Напишите ионно-молекулярные и молекулярные уравнения гидролиза соли. Выведите и рассчитайте Kгидр по 1- и 2-й ступени, а также степень гидролиза и pH раствора для 1 ступени гидролиза при заданной концентрации
«Напишите ионно-молекулярные и молекулярные уравнения гидролиза соли. Выведите и рассчитайте Kгидр по 1- и 2-й ступени, а также степень гидролиза и pH раствора для 1 ступени гидролиза при заданной концентрации»
- Химия
Условие:
Напишите ионно-молекулярные и молекулярные уравнения гидролиза соли. Выведите и рассчитайте Kгидр по 1- и 2-й ступени, а также степень гидролиза и pH раствора для 1 ступени гидролиза при заданной концентрации.
KCN – соль одноосновных сильного основания (KOH) и слабой кислоты (HCN), гидролиз по аниону в одну ступень.
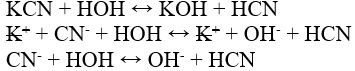
Решение:
Исходные данные:
СKCN = 0,5 моль/л.
= 1,12 г/мл.
Найти: Кг-?, h-?, рН-?
Решение:
Ионное произведение воды:
KW = [H+]∙[OH-] = 1∙10-14.
Константа диссоциации слабой кислоты (справочные данные):
HCN H+ + CN-
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э