Напишите математическое выражение 2-го закона термодинамики в дифференциальной форме для обратимого (равновесного) и необратимого процессов в открытой системе.
- Химия
Условие:
Второе начало термодинамики.
Энтропия. Термодинамические потенциалы
1. Напишите математическое выражение 2-го закона термодинамики в дифференциальной форме для обратимого (равновесного) и необратимого процессов в открытой системе.
2. Энтропия как критерий состояния равновесия и направления протекания самопроизвольного процесса в изолированной системе.
3. Напишите уравнения, выражающие зависимость энтропии от температуры (p=const) и давления (T=const). Приведите уравнения для расчета изменения энтропии в изобарном, изохорном и изотермическом процессах с участием идеального двухатомного газа.
4. Рассчитайте изменение энтропии (DS01) вещества А (табл. 1) при изобарном нагревании от 298 до 800 K в Дж/моль·К. (Принять, что вещество А находится в газообразном состоянии, используйте уравнение
Cp0 = f(T) (см. задание 1, п.15).
5. На основании уравнения зависимости теплоемкости от температуры Cp0 = f(T) (п. 4) рассчитайте значения теплоемкости C0p,А для газообразного вещества А при температурах 298, 400, 500, 700, 800 и 1000 K.
6. Используя значения C0p,А, рассчитанные в п.5, постройте график зависимости C0p/Т = f(T) для вещества А, находящегося в газообразном состоянии.
7. Графическим интегрированием определите изменение энтропии вещества А при изобарном нагревании от 298 до 800 K в Дж/моль·К.
8. Определите абсолютную энтропию S0800 вещества A на основании значения S0298 [1] и DS01.
9. Определите изменение энтропии (DS02) вещества А в Дж/моль·К в процессе изменения давления от р1 до р2 при температуре 800 K. p1 = 1,013·105 Па, p2 = 0,2533·105 Па.
10. Определите абсолютную энтропию вещества А в Дж/моль·К при 800 К и давлении р2.
11. Определите изменение энтропии (DrS0298) для реакции А (см. задание 1), протекающей при 298 К и стандартном давлении.
СО2 + 4Н2 = СН4 + 2Н2О
12. Укажите при каких условиях проведения процесса DG и DA служат критериями состояния равновесия и направления самопроизвольного протекания процесса. Приведите соответствующие выражения.
13. Напишите уравнение, выражающее зависимость энергии Гиббса от давления и температуры в дифференциальной форме. Приведите графические зависимости G = f(p) при T = const и G = f(T) при T = const.
14. Приведите уравнения для расчета изменения энергии Гиббса при изотермическом расширении от давления р1 до р2 и изобарном нагревании от Т1 до Т2 1 моль газа в идеальном состоянии.
15. Рассчитайте изменение энергии Гиббса (DG1) при изобарном нагревании (p1 =1,013·105 Па) 1 моль вещества А, находящегося в идеальном газообразном состоянии, от T1 = 298 K до T2 = 800 K в кДж/моль (принять, что энтропия не зависит от температуры и равна S0298).
16. Рассчитайте изменение энергии Гиббса (DG2) в процессе изотермического расширения 1 моль вещества А, находящегося в идеальном газообразном состоянии, от давления p1 =1,013·105 Па до p2 =0,2533·105 Па при температуре 800 K в кДж/моль.
17. Определите ΔG для 1 моль вещества А, при изменении давления от p1 =1,013·105 Па до p2 =0,2533·105 и одновременном изменении температуры от 298 до 800 К в кДж/моль. Вещество А находится в идеальном газообразном состоянии.
18. Определите DG0298 в кДж для реакции А (см. задание 1), протекающей при Т = 298 К, и сделайте вывод о направлении реакции.
19. Определите DrА0298 в кДж для реакции А, протекающей при Т = 298 K, и сделайте вывод о направлении реакции.
20. Определите DrG0298 в кДж для реакции А для случая, когда все реагенты являются идеальными газами.
Решение:
1.Выражение 2-го закона термодинамики в дифференциальной форме: для обратимого (равновесного) процесса: 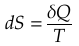 для необратимого процесса:
для необратимого процесса: 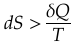 .
.
2.Изменение энтропии является критерием направления процесса в из...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства