Подберите коэффициенты в уравнении реакции PH3 + KMnО4 + H2SО4 → H3PО4 + MnSО4 + K2SО4 + H2О двумя методами: ионно-электронным и балансовым. Укажите окислитель и восстановитель.
«Подберите коэффициенты в уравнении реакции
PH3 + KMnО4 + H2SО4 → H3PО4 + MnSО4 + K2SО4 + H2О
двумя методами: ионно-электронным и балансовым. Укажите окислитель и восстановитель.»
- Химия
Условие:
Подберите коэффициенты в уравнении реакции
PH3 + KMnО4 + H2SО4 → H3PО4 + MnSО4 + K2SО4 + H2О
двумя методами: ионно-электронным и балансовым. Укажите окислитель и восстановитель.
Решение:
а) метод ионно-электронного баланса.
PH3 + KMnО4 + H2SО4 H3PО4 + MnSО4 + K2SО4 + H2О.
Запишем уравнение реакции в ионно-молекулярном виде:
PH3 + K+ + MnО4- + 2H+ + SО42- H3PО4 + Mn2+ + SО42- + 2K+ + SО42- + H2О.
Изменяют форму существования в растворе:
PH3 на H3PО4 и MnО4- - на Mn2+.
Запишем ионно-электронные уравнения.
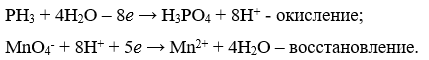
Наименьшее кратное для чисел 8 и 5 равно 40.
Р...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э