Условие:
После растворения навески оксида железа массой 0,1000 г и восстановления железа до Fe2+ на титрование израсходовали 12,61 мл 0,09931 н. раствора K2Cr2O7 (f = 1/6). Определить формулу анализируемого оксида: FeO, Fe2O3, Fe3O4?
Дано: 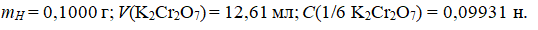
Найти: ω(Fe) - ?
Решение:
В ходе титрования идёт реакция
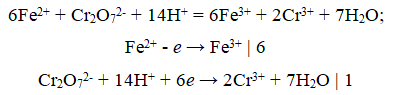
По закону эквивалентов
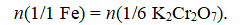
Число молей эквивалентов железа равно
