Условие задачи
При определении Na2SO4 в растворе методом йодометрии ионы SO42- путем ряда превращений заменили эквивалентным количеством CrO42-. Раствор подкислили, прибавили KI и выделившийся I2 оттитровали 20,40 мл 0,01980 М раствором Na2S2O3. Какая масса Na2SO4 содержалась в исследуемом растворе?
Дано: V(Na2S2O3) = 20,40 мл; СМ(Na2S2O3) = 0,01980 моль/л.
Найти: т(Na2SO4) - ?
Ответ
По условию задачи
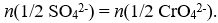
При подкислении раствора хромат-ионы превращаются в бихромат-ионы:
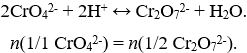
При взаимодействии с раствором KI идёт реакция