При синтезе аммиака N2(г) + 3H2(г) ⇆ 2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ, моль/л : [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
«При синтезе аммиака N2(г) + 3H2(г) ⇆ 2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ, моль/л : [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.»
- Химия
Условие:
При синтезе аммиака N2(г) + 3H2(г) ⇆ 2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ, моль/л : [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение:
Константа равновесия реакции
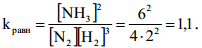
Начальная концентрация вещества складывается из равновесной концентрации этого вещества и количества вещества, израсходованного на образование равновесной концентрации продукта реакции. На основе уравнения реакции определяем количество израсходованного N2:
на образование 2 моль NH3 расходуется 1 моль N2; на образование 6 ...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э