Применяя принцип Ле Шателье и уравнений, определите как будет меняться равновесный выход конечных продуктов реакции при: повышении температуры; понижении температуры; повышении давления; понижении давления. цоцл два равно цо плюс цлдва.
«Применяя принцип Ле Шателье и уравнений, определите как будет меняться равновесный выход конечных продуктов реакции при: повышении температуры; понижении температуры; повышении давления; понижении давления. цоцл два равно цо плюс цлдва.»
- Химия
Условие:
Применяя принцип Ле Шателье и уравнений, определите как будет меняться равновесный выход конечных продуктов реакции при: а) повышении температуры; б) понижении температуры; в) повышении давления; г) понижении давления; д) добавлении инертного газа.
COCl2=CO+Cl2
Решение:
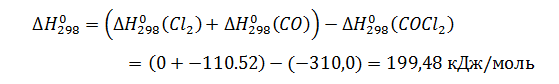
△Н0, реакция эндотермическая
а) При повышении температуры равновесие сдвигается в сторону эндотермической реакции, в сторону исходн...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э