Условие:
Применяя принцип Ле Шателье и уравнения (XVII.3) и (XVII.30), определите, как будет меняться равновесный выход конечных продуктов реакции при:
а) повышении температуры;
б) понижении температуры;
в) повышении давления;
г) понижении давления;
д) добавлении инертного газа.
2SO2 + O2 = 2SO3
Решение:
По закону Гесса определим тепловой эффект данной реакции при 298 К:
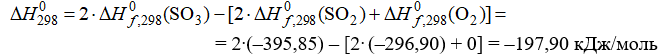
Так как 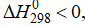 то прямая реакция экзотермическая, а обратная реакция эндотермическая.
то прямая реакция экзотермическая, а обратная реакция эндотермическая.
Константа равновесия реакции имеет вид:
