Рассчитайте экобаланс производства хлора для обеззараживания воды расход которой составил Q, если вводят дозу хлора X. Хлор производят методом электролиза раствора поваренной соли с концентрацией
- Химия
Условие:
Рассчитайте экобаланс производства хлора для обеззараживания воды расход которой составил Q, если вводят дозу хлора X. Хлор производят методом электролиза раствора поваренной соли с концентрацией 300 г/дм3. Плотность раствора 1,17 кг/дм3. Степень разложения соли – Y. Частично хлор растворяется в конечном растворе с образованием гипохлорита натрия, его концентрация – C. Данные для решения задачи приведены в табл. 3.8 по вариантам.
Т а б л и ц а 3.8. Данные для задачи 3.8
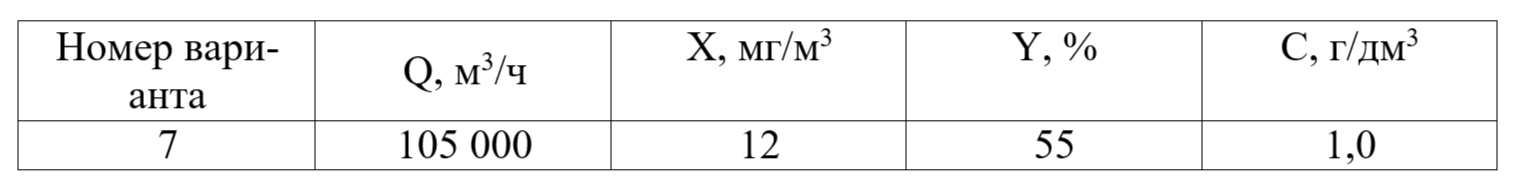
Решение:
Рассчитаем количество хлора: 215000 м3 /ч∙0,012 г/м3 = 2580 г/ч = 2,58 кг/ч.
Процесс электрохимического синтеза Cl2 протекает по реакции:
2NaCl + 2H2O Cl2 + H2 + 2NaOH,
а образование побочного продукта по реакции:
Cl2 + 2NaOH = NaCl + NaClO + H2O.
Для получения 2,58 кг/с Cl2 по первой реакции расходуется NaCl (молярная масса 58,5) в количестве:
mNaCl=(2,58∙2∙58,5)/71=4,25 кг
При учете степени разложения NaCl 55 % требующаяся масса соли составляет:
mисх=4,25/0,55=7,73 кг
Объем раствора:
V=(7,73 )/300=0,026 м3/ч
а его масса m = 0,026 * 1170 = 30,1...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства