Рассчитайте, как изменятся скорости прямой и обратной реакций в системе 2SO2 + O2 = 2SO3, если уменьшить объем, занимаемый газами, в два раза. Сместится ли при этом равновесие системы?
«Рассчитайте, как изменятся скорости прямой и обратной реакций в системе 2SO2 + O2 = 2SO3, если уменьшить объем, занимаемый газами, в два раза. Сместится ли при этом равновесие системы?»
- Химия
Условие:
Рассчитайте, как изменятся скорости прямой и обратной реакций в системе 2SO2 + O2 = 2SO3, если уменьшить объем, занимаемый газами, в два раза.
Сместится ли при этом равновесие системы?
Решение:
Согласно закону действующих масс скорости прямой и обратной реакций выражаются следующим образом:
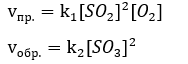
При уменьшении объема, занимаемого газами, в два раза концентрация каждого из реагирующих веществ увеличивается так же в два раза.
С учетом уменьшения давления...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э