Рассчитайте константу равновесия реакции и исходные концентрации азота и водорода.
- Химия
Условие:
При синтезе аммиака ![]() равновесие установилось при следующих концентрациях реагирующих веществ:
равновесие установилось при следующих концентрациях реагирующих веществ: ![]() =4 моль/л,
=4 моль/л, ![]() =2 моль/л,
=2 моль/л, 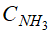 =6 моль/л. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
=6 моль/л. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение:
Константа равновесия этой реакции равна:Исходные концентрации азота и водорода находим на основе уравнения реакции. На образование двух молей NH3 расходуется один моль N2, а на образование шести молей аммиака потребовалось: 6/2=3 моль азота.Учитывая равновесную концентрацию азота, находим его первоначальную концентрацию: На образование двух молей NH3 необходимо израсходовать 3 моль водорода, а для получения шести молей NH3 требуется водорода: (3*6) / 2 = 9 моль:Таким образом, реакция начиналась при 7 моль/л; = 11 ...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства