Рассмотрите все возможные взаимодействия в системах: А) Cu + HNO3 (конц.) Б) Cu + HCl В) Zn + Al2(SO4)3 + H2O. Для окислительно-восстановительных процессов рассчитать значение эдс.
«Рассмотрите все возможные взаимодействия в системах: А) Cu + HNO3 (конц.) Б) Cu + HCl В) Zn + Al2(SO4)3 + H2O. Для окислительно-восстановительных процессов рассчитать значение эдс.»
- Химия
Условие:
Рассмотрите все возможные взаимодействия в системах:
А) Cu + HNO3 (конц.)
Б) Cu + HCl
В) Zn + Al2(SO4)3 + H2O
Для окислительно-восстановительных процессов рассчитать значение эдс.
Решение:
А) Cu + HNO3 (конц.)
ECu2+/Cu = +0,34B;
E2H+/H2 = 0 B
ENO3-/NO2 = 0,77В
Восстановитель- медь, окислитель нитрат ионы
Cu + HNO3 (разб.) Cu(NO3)2 + NO2 + H2O
Cu0 + H+ + NO3- Cu2+ + 2NO3- + NO2 + H2O
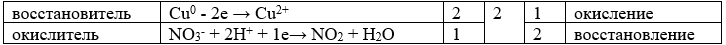
Cu0 + 2NO3- + 4H+ Cu2+ + 2NO2 + 2H2O
Cu + 4HNO3 (разб.) Cu(NO3)2 + 2NO2 +2H2O
Стандартная ЭДС реакции равна:
ЭДС = Еокисл - Евосст
ЭДС = Е(NO3-/ NO2) - Е( Cu2+/ Cu0) = 0,77...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э