Решение задачи по расчету реактора окисления диоксида серы. Окисление диоксида серы проводят в адиабатическом реакторе полного смешения. Состав исходной смеси (об. доли): диоксид серы - 0,07, кислород - 0,13, триоксид серы
- Химия
Условие:
Решение задачи по расчету реактора окисления диоксида серы.
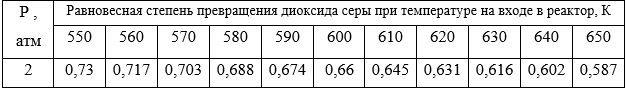
Окисление диоксида серы проводят в адиабатическом реакторе полного смешения. Состав исходной смеси (об. доли): диоксид серы - 0,07, кислород - 0,13, триоксид серы - 0, остальное - азот. Изменение равновесной степени превращения диоксида серы от температуры реакционной смеси представлено в таблице:
Зависимость константы скорости от температуры:
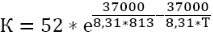
Зависимость константы равновесия от температуры:
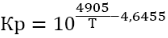
Кинетическое уравнение:
![]() ,
,
где PSO2, PSO3, PO2 - текущие парциальные давления диоксида серы, триоксида серы и кислорода.
Расход исходной газовой смеси 45000 м3/ч.
Температура на входе в реактор 620 K.
Давление в реакторе 2 атм.
Степень превращения диоксида серы составляет 0,85 от равновесного значения.
Рассчитать требуемый объѐм реактора, производительность по триоксиду серы и температуру на выходе из реактора.
Решение:
1. Рассчитываем конечную степень превращения диоксида серы используя данные таблицы:
Х = 0,85·0,73 = 0,62 .
2. Рассчитываем конечные мольные доли диоксида серы, триоксида серы и кислорода:
ZSO2 = 0,07 · 0,62 / (1 0,5 · 0,07 · 0,62) = 0,044 ;
ZO2 = (0,13 0,5 · 0,07 · 0,62) / (1 0,5 · 0,07 · 0,62) = 0,111 ;
ZSO3 = (0 + 0,07 · 0,62) / (1 0,5 · 0,07 · 0,62) = 0,044 .
3. Рассчитываем конечные парциальные давления компонентов:
PSO2 = 2 · 0,044 = 0,088;
PO2 = 2 · 0,111 = 0,222;
PSO3 = 2 · 0,044 = 0,088.
4. Рассчитываем и...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства