Решите следующую задачу: вычислить растворимость в (моль/л) СаF два в воде; в ноль целых три сотых М растворе HCl; в ноль целых одна десятая М растворе СаCl два.
«Решите следующую задачу: вычислить растворимость в (моль/л) СаF два в воде; в ноль целых три сотых М растворе HCl; в ноль целых одна десятая М растворе СаCl два.»
- Химия
Условие:
Вычислить растворимость в (моль/л) СаF2 в воде; в 0,03М растворе HCl; в 0,1М растворе СаCl2. (ПР(СаF2) = 4∙10-11).
Решение:
Незначительная часть CaF2 переходит в растворенное состояние:
В воде:
CaF2 ⇄ Ca2+ + 2F-
ПР = [Ca2+][F-]2
[Сa2+] = s [F-] = 2s
ПР = s (2s)2 = 4s3
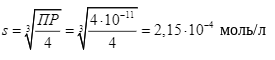
В растворе HCl необходимо учитывать ионную силу раствора:
HCl = H+ + Cl-
ПР = a(Ca2+) ∙ a2(F-)
Так как концентрация ионов фторида кальц...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э