Смесь карбонатов магния и бария растворили в избытке азотной кислоты. Выделился газ. При действии избытка серной кислоты на полученный раствор образовался осадок. Рассчитайте массовые доли веществ в исходной смеси.
«Смесь карбонатов магния и бария растворили в избытке азотной кислоты. Выделился газ. При действии избытка серной кислоты на полученный раствор образовался осадок. Рассчитайте массовые доли веществ в исходной смеси.»
- Химия
Условие:
Смесь карбонатов магния и бария растворили в избытке азотной кислоты. Выделился газ объёмом 13,44 л (н.у.). При действии избытка серной кислоты на полученный раствор образовался осадок массой 46,6 г. Рассчитайте массовые доли (в %) веществ в исходной смеси. (46%, 54%)
Решение:
Дано:
MgCO3 + BaCO3 + HNO3(изб)
V(газа) = 13,44 л
m( осадка) = 46,6 г
Найти : массовые доли исходных веществ - ?
1.При действии избытка азотной кислоты на карбонаты :
MgCO3 +2 HNO3 = Mg(NO3)2 + CO2 + H2O
BaCO3 +2 HNO3 = Ba(NO3)2 + CO2 + H2O
Далее подействовали серной кислотой:
Ba(NO3)2 + H2SO4 = BaSO4 + 2HNO3
Количество вещества сульфата бария:
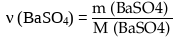
M(BaSO4) = 137 + 32 + 4∙ 16 = 233 г/моль молярная масса суль...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э