Составьте электродные уравнения процессов, происходящих на растворимых электродах (см. исходные данные в табл.). Укажите реакцию среды раствора (рН) до электролиза и изменение рН у анода и катода в процессе электролиза.
- Химия
Условие:
1. Составьте электродные уравнения процессов, происходящих на инертных электродах, при электролизе водного раствора соли и при заданных условиях (сила тока (гафа 2) и время (графа 3)) (см. исходные данные в табл.). Вычислите массы (и объемы, если вещества газообразные) веществ, выделившихся на катоде и аноде при 100% выходе по току на катоде и 95% – на аноде.
2. Составьте электродные уравнения процессов, происходящих на растворимых электродах. Укажите реакцию среды раствора (рН) до электролиза и изменение рН у анода и катода в процессе электролиза.

Решение:
Электролиз раствора AgNO3:
K: Ag+ + e Ag |2
A: 2H2O O2 + 4H+ + 4e |1
Вывод: 2AgNO3 + 2H2O 2Ag + O2 + 2HNO3
По законам Фарадея:
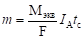
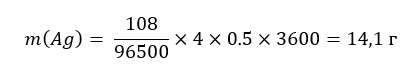
По законам Фарадея объем выделившегося кислорода:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства