Условие:
Составьте схему гальванического элемента, в основе которого лежит реакций, протекающая по уравнению Ni + Pb(NO3)2 = Ni(NO3)2 + Pb.
Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элемента, если [Ni2+] = 0,01 моль/л, [Pb2+] = 0,0001 моль/л.
Дано: [Ni2+] = 0,01 моль/л, [Pb2+] = 0,0001 моль/л.
Найти: Е - ?
Решение:
0(Ni2+/Ni0) = - 0,250 В; 0(Pb2+/Pb0) = -0,126 В.
По уравнению Нернста вычисляем потенциалы с учетом концентраций растворов:
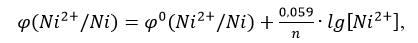
где 0(Ni2+/Ni0) стандартный электродный потенциал, равен - 0,250 В;
n число электронов, равно 2;
[Ni2+] м...
![Составьте схему гальванического элемента, в основе которого лежит реакций, протекающая по уравнению Ni + Pb(NO3)2 = Ni(NO3)2 + Pb. Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элемента, если [Ni2+] = 0,01 моль/л,](/public/images/library/external/library-detail-hero-book.png)