Составьте схемы электролиза и рассчитайте массу металла, выделяющегося на катоде, по приведенным данным при 3-х разных условиях его проведения:
- Химия
Условие:
Составьте схемы электролиза и рассчитайте массу металла, выделяющегося на катоде, по приведенным данным при 3-х разных условиях его проведения:
- из раствора соли металла, при использовании растворимого анода.
- из раствора соли металла, при использовании нерастворимого анода.
- из расплава соли металла, при использовании растворимого анода.
Формула соли MnSO4
I, A 1,9
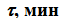 45
45
ВТ, % масс. 25
Решение:
Электролиз водных растворов электролитов осложняется участием в электродных процессах молекул воды.
1. Катионы металлов от Li+ до Al3+ включительно (Е0Меn+/Ме0 1,66 В) не восстанавливаются на катоде, вместо них на катоде восстанавливаются молекулы воды в соответствии с уравнением реакции:
2Н2О + 2е = Н2 + 2ОН
2. Катионы металлов от Mn2+ до H, восстанавливаются на катоде вместе с молекулами воды:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства