Условие:
Уравняйте окислительно-восстановительную реакцию, определите окислитель и восстановитель реакции, а так же направление ее протекания.
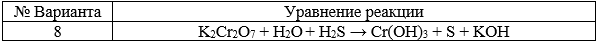
Решение:
K2Cr2O7 + H2O + H2S Cr(OH)3 + S + KOH
В ходе данной окислительно-восстановительной реакции хром и сера меняют свои степени окисления. Вода обуславливает нейтральную среду. Составим уравнения полуреакций:
Cr2O72- + 7H2O + 6e- 2Cr(OH)3 + 8OH‑ | 1 окислитель, процесс восстановления
H2S 2e- S0 + 2H+ | 3 восстановитель, процесс окисления
Суммируем полученные полуреакции, домножая каждую на подобранный коэффициент:
Cr2O72- + 7H2O + 3H2S 2Cr(OH)3 + 8OH‑ + 3S0 + 6H+
Итоговое уравнение с учетом подобранных коэффициентов:
K2Cr2O7 + H2O + 3H2S = 2Cr(OH)3 + 3S + 2KOH
K2Cr2...
