В табл. 7 приведены значения констант скоростей k1 и k2 реакции при двух различных температурах T1 и T2. Вычислите: а) энергию активации данной реакции;
- Химия
Условие:
В табл. 7 приведены значения констант скоростей k1 и k2 реакции при двух различных температурах T1 и T2.
Вычислите:
а) энергию активации данной реакции;
б) рассчитайте константу скорости при температуре T3;
в) определите степень протекания процесса (долю прореагировавшего вещества) к моменту времени t, если известна начальная концентрация вещества c0 (c0 – начальные концентрации реагирующих веществ одинаковы) и порядок реакции равен молекулярности;
г) определите по правилу Вант-Гоффа температурный коэффициент константы скорости реакции и проверьте применимость правила.
Таблица 7

Решение:
а) Для определения энергии активации воспользуемся уравнением Аррениуса в интегральной форме:
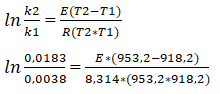
1,572 = 0,000004809*Е
Е = 326887 Дж/моль
б) Для определения константы скорости при заданной температуре Т3 = 988,2 К воспользуемся интегральной формой уравнения Аррениуса, зная энергию активации:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства