Условие:
В уравнениях окислительно-восстановительных реакций расставьте коэффициенты. Для реакции а) используйте метод электронного баланса, а для реакции б) – ионно-электронный метод. В каждой реакции определите окислитель и восстановитель. Вычислите ЭДС и константу равновесия реакции б). Определите направление и полноту протекания реакции в стандартных условиях. Значения стандартных электродных окислительно-восстановительных потенциалов приведены в прил., табл. П.5.
а) FeS2 + O2 → Fe2O3 + SO2
б) K2Cr2О7 + Н2S + Н2SО4 → S + Сr2(SO4)3 + K2SO4 +H2O
Таблица П.5
Стандартные электродные окислительно-восстановительные потенциалы φ0 в водных растворах при 25 °С
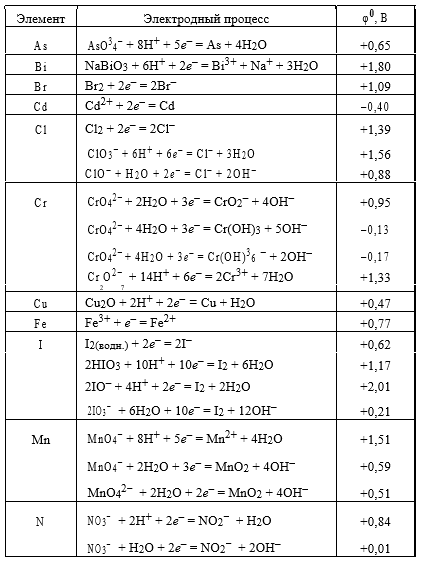
Решение:
а) 4FeS2+11O2=2Fe2O3+8SO2
2Fe+2 -2e=2Fe+3 x2 восстановитель; окисление
O20 +4e=2O-2 x1 окислитель; восстановление
FeS2 восстановитель; O2 окислитель.
б) K2Cr2О7 + Н2S + Н2SО4 S + Сr2(SO4)3 + K2SO4 +H2O
Cr2O72-+14H+ +6e=2Cr3++7H2O x1 окислитель; восстановление
H2S -2e =S+2H+...
