а) определите молярную концентрацию 60%-ного раствора серной кислоты (ρ = 1,50 г/мл); б) сколько миллилитров 32-процентного раствора азотной кислоты (ρ = 1,19 г/мл) требуется для приготовления 300 мл 0,75 М раствора?
«а) определите молярную концентрацию 60%-ного раствора серной кислоты (ρ = 1,50 г/мл); б) сколько миллилитров 32-процентного раствора азотной кислоты (ρ = 1,19 г/мл) требуется для приготовления 300 мл 0,75 М раствора?»
- Химия
Условие:
а) определите молярную концентрацию 60%-ного раствора серной кислоты (ρ = 1,50 г/мл);
б) сколько миллилитров 32-процентного раствора азотной кислоты (ρ = 1,19 г/мл) требуется для приготовления 300 мл 0,75 М раствора?
Решение:
а)Дано:
W(H2SO4)=60%
(р-ра)=1,50 г/мл
С(H2SO4) - ?
Находим молярную концентрацию раствора карбоната натрия:
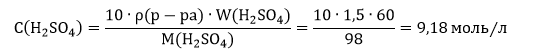
Ответ: С(H2SO4)=9,18 моль/л.
б)Дано:
V2(р-ра)=300 мл=0,3 л
С2(HNO3)=0,7...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э