Условие:
Вычислите рН 0,05 М раствора HNO3 и 0,05 М раствора СН3СООН. Объясните различия в значениях. Напишите уравнения ступенчатой диссоциации Н3РО4 и выражения для константы диссоциациипо второй ступени.
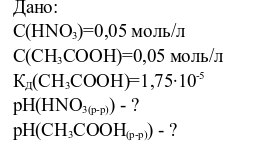
Решение:
Находим концентрацию ионов водорода в растворе азотной кислоты:
поскольку HNO3 сильный электролит, то в водном растворе диссоциирует полностью:
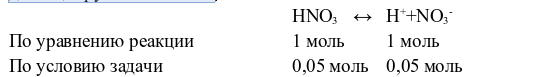
Следовательно, [H+]=0,05 моль/л.
Находим рН раствора азотной кислоты:
