Вычислите температуру, при которой будут равновероятны оба направления реакции CH4(г) + CO2(г) = 2CO(г) + 2H2(г). Как надо изменить температуру, чтобы увеличить вероятность протекания прямой реакции?
«Вычислите температуру, при которой будут равновероятны оба направления реакции CH4(г) + CO2(г) = 2CO(г) + 2H2(г). Как надо изменить температуру, чтобы увеличить вероятность протекания прямой реакции?»
- Химия
Условие:
Вычислите температуру, при которой будут равновероятны оба направления реакции
CH4(г) + CO2(г) = 2CO(г) + 2H2(г).
Как надо изменить температуру, чтобы увеличить вероятность протекания прямой реакции?
Решение:
Справочные данные, необходимые для расчета (по справочнику Равделя):
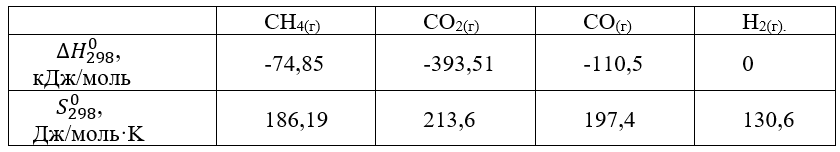
Согласно следствию из закона Гесса находим изменение энтальпии для данной химической реакции:
![]() с учетом стехиометрии
с учетом стехиометрии
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э