Запишите выражение для скорости данной реакции (закон действующих масс для химической кинетики). На основании известных данных о концентрациях участников реакции вычислите, во сколько раз уменьшилась начальная скорость реакции спустя время.
- Химия
Условие:
Кинетические измерения показали, что реакция
2NO + O2 = 2NO2
имеет третий порядок. В начальный момент времени концентрации исходных веществ равны [NO]0 и [O2]0. Спустя некоторый промежуток времени t концентрации исходных веществ уменьшаются на ∆[NO] и ∆[O2] и становятся равными [NO] и [O2], вследствие чего скорость реакции уменьшается.
Запишите выражение для скорости данной реакции (закон действующих масс для химической кинетики). На основании известных данных о концентрациях участников реакции вычислите, во сколько раз уменьшилась начальная скорость реакции спустя время t.
Исходные данные: [O2]0 = 3,5 моль/л; ∆[O2] = 0,5 моль/л; [NO] = 2,3 моль/л.
Решение:
Дано: [O2]0= 3,5 моль/л; ∆[O2] = 0,5 моль/л; [NO] = 2,3 моль/л.
Найти: 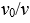 - ?
- ?
2NO + O2 = 2NO2
Скорость реакции равна
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства