1. Вычислите степень гидролиза карбоната натрия в растворе с рН = 12. 2. Вычислите изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли, после добавления к 1 л раствора 0,1 моль соляной кислоты.
«1. Вычислите степень гидролиза карбоната натрия в растворе с рН = 12. 2. Вычислите изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли, после добавления к 1 л раствора 0,1 моль соляной кислоты.»
- Химия
Условие:
1. Вычислите степень гидролиза карбоната натрия в растворе с рН = 12.
2. Вычислите изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли, после добавления к 1 л раствора 0,1 моль соляной кислоты.
Решение:
1.
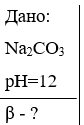
Составим ионное уравнение первой ступени гидролиза соли по аниону:
CO32- + H2O HCO3- + OH-
Это первая ступень гидролиза а соответствующая константа гидролиза Kh1 определяется значением константы диссоциации, образующегося при гидролизе аниона (НСО3-), т.е. второй константой диссоциации угольной кислоты Н2СО3 Кd2 = 4,69*10-11.
Первую константу гидролиза найдем из выражения:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э