Для обратимой химической реакции охарактеризуйте состояние химического равновесия и возможность его смещения.
- Химия
Условие:
Для обратимой химической реакции охарактеризуйте состояние химического равновесия и возможность его смещения.
1. Напишите выражение константы химического равновесия.
2. Укажите, как следует изменить:
– температуру;
– давление;
– концентрацию исходных веществ;
– концентрацию продуктов реакции,
чтобы сместить равновесие в сторону прямой реакции (повысить выход продуктов реакции).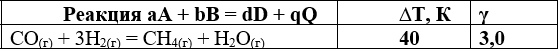
Решение:
1) Обратимая химическая реакция протекает в прямом или обратном направлении до состояния химического равновесия.
Химическое равновесие наступает в системе, если достигаются условия: кинетическое скорости прямой и обратной реакции равны uпр = uобр ; термодинамическое при Т = const и Р = const ; концентрационное концентрации веществ постоянны, C= const.Закон действующих масс применяется и для обратимых химических реакций в виде выражения константы химического равновесия К.Для обратимой гомогенной химической реакции аА + bВ ⇄ dD + qQ
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства