При какой концентрации ионов S 2− произойдет выпадение осадка FeS из 0,003 М раствора К4[Fe(CN)6], содержащего 0,01 моль KCN в 2 л раствора? ПР(FeS) = 3,7∙10−19 ; Кн[Fe(CN)6] 4− = 1,0∙10−24
«При какой концентрации ионов S 2− произойдет выпадение осадка FeS из 0,003 М раствора К4[Fe(CN)6], содержащего 0,01 моль KCN в 2 л раствора? ПР(FeS) = 3,7∙10−19 ; Кн[Fe(CN)6] 4− = 1,0∙10−24»
- Химия
Условие:
При какой концентрации ионов S 2− произойдет выпадение осадка FeS из 0,003 М раствора К4[Fe(CN)6],
содержащего 0,01 моль KCN в 2 л раствора? ПР(FeS) = 3,7∙10−19 ; Кн[Fe(CN)6] 4− = 1,0∙10−24
Решение:
Kн комлексной соли 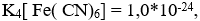
В растворе комплексная соль диссоциирует
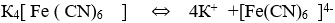
концентрация соли в 2 л 0.003 М растворе составляет 0.0015 моль, /л при диссоциации этой соли образовывается 0.0015*4=0.006моль катионов K+ и...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э