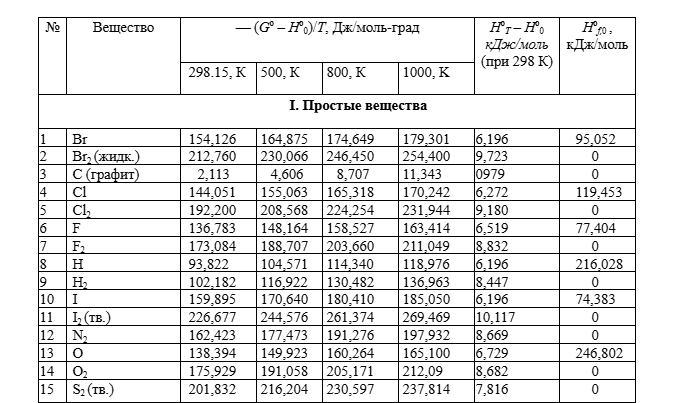
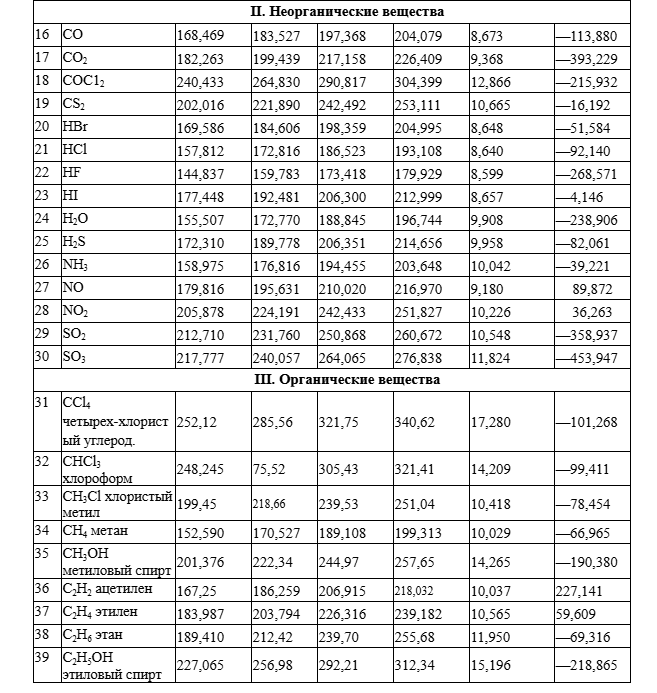
Условие:
- Для данной реакции 2Н2О = 2Н2 + О2 в приведенном температурном интервале (298, 500, 800, 1000 К) на основании справочных данных приведенной энергии Гиббса и высокотемпературных составляющих энтальпии определите значения ΔrGo(T), ΔrHo(T), ΔrSo(T), Kp(T) и Kс(T).
- Определите значения вышеперечисленных термодинамических параметров данной реакции без учета зависимости ΔrHo (298) и ΔrSo (298) от температуры.
- Запишите выражения для констант равновесия Kp и Kс в зависимости от равновесных парциальных давлений и концентраций реагентов.
- По полученным данным сделайте заключение о зависимости вышеперечисленных термодинамических параметров от температуры и смещении химического равновесия.
- Определите погрешность в значениях термодинамических параметров без учета температурной зависимости.