По значениям констант скоростей реакции 2HI → H2 + I2 определите: температурный коэффициент скорости реакции (по правилу Вант-Гоффа); энергию активации Е; константу скорости k3 при температуре Т3.
- Химия
Условие:
По значениям констант скоростей реакции
2HI → H2 + I2
при двух температурах определите:
1) температурный коэффициент скорости реакции (по правилу Вант-Гоффа);
2) энергию активации Е;
3) константу скорости k3 при температуре Т3;
4) число общих столкновений в 1 л за 1 с (предэкспотенциальный множитель k0 в уравнении Аррениуса) при Т3;
5) долю активных столкновений 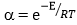 при Т3;
при Т3;
6) сделать вывод из сопоставления общих и активных столкновений.
Исходные данные: Т1 = 666К; k1 = 2,19*10-4 л/(моль*с); Т2 = 683К; k2 = 5,12*10-4 л/(моль*с); Т3 = 675К
Решение:
Дано: Т1 = 666К; k1 = 2,19*10-4 л/(моль*с); Т2 = 683К; k2 = 5,12*10-4 л/(моль*с); Т3 = 675К
1) Согласно правилу Вант-Гоффа:
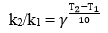
откуда путем логарифмирования выразим :
lg(k2/k1) = (T2 T1)*lg/10;
lg = 10*lg(k2/k1)/(T2 T1);
lg = 10*lg(5,12*10-4 /2,19*10-4) / (683 - 666) = 0,217
= 100,217 = 1,65.
2) Энергию активации вычислим из уравнения Аррениуса:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства