Условие:
1. Используя термодинамические справочные данные («Краткий справочник физико-химических величин» под редакцией А.А. Равделя), рассчитайте ∆H298о, ∆G298о и ∆S298о реакции:
СаСО3(к) = СаО(к) + СО2(г).
Укажите направление протекания процесса при 298К и объясните знак изменения энтропии реакции.
2. Полагая, что изменение энтропии и энтальпии реакции не зависят от температуры, определите температуру, при которой константа равновесия рассматриваемой реакции окажется равной единице.
3.Укажите, в какую сторону сместится равновесие рассматриваемой реакции при повышении температуры и понижении давления. Ответ обосновать.
Решение:
1. Выпишем стандартные значения энтальпий образования веществ Hf 298, энтропий веществ S298 и значения энергий Гиббса образования веществGf 298 :
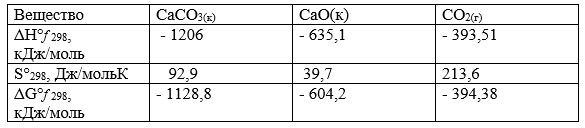
а) Вычислим стандартное изменение энтальпии химической реакции ∆Н0298
Согласно следствию из закона Гесса, стандартное изменение энтальпии химической реакции равно разности между суммой энтальпий образования продуктов реакции и суммой энтальпий...
