Условие:
1. Какая масса природного известняка, содержащего 90% карбоната кальция, потребуется для получения 7 г негашёной извести?
2. Определите молярную концентрацию раствора соляной кислоты, рН которого paвен 2, считая диссоциацию электролита полной.
Решение:
1.
Дано:
W(CaCO3) = 90 %
m(CaO)=7 г
m(известняка) - ?
Находим массу карбоната кальция, который необходим для получения 7 г негашеной извести:
CaCO3 CaO+CO2
По уравнению реакции 100 г 56 г
По условию задачи х г 7 г
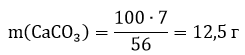
Находи...
