Решение задачи
1. Какова истинная формула соединения, содержащего 6,75 процентов водорода, 39,97 процентов углерода и кислород. Относительная плотность паров этого вещества по оксиду углерода
- Химия
Условие:
1. Какова истинная формула соединения, содержащего 6,75 % водорода, 39,97 % углерода и кислород. Относительная плотность паров этого вещества по оксиду углерода (IV) равна 4,091.
2. Вычислить объёмные доли (в процентах) неона и аргона в смеси, если их парциальное давление соответственно 203,4 и 24,6 кПа.
Решение:
1.
Дано:
W(H) = 6,75 %
W(C) = 39,97 %
DCO2(CXHYOz) = 4,091
CXHYOz - ?
Находим массовую долю кислорода в неизвестном соединении:
W(O) = 100% - (W(H) + W(C)) = 100% - (6,75 + 39,97) = 53,28%
Находим соотношение атомов углерода, водорода и кислорода в простейшей формуле неизвестного соединения:
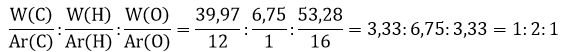
Cледовательно, простейшая формула соединения имеет вид СН2О.
Находим относительную молекулярную массу неизве...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э