Условие:
1. Сколько металла, эквивалентная масса которого 12,16 г/моль, взаимодействует с 310 см3 (мл) кислорода, н.у.?
2. Из 3,85 г нитрата металла получено 1,6 г его гидроксида. Вычислите молярную массу эквивалентов металла.

1. Сколько металла, эквивалентная масса которого 12,16 г/моль, взаимодействует с 310 см3 (мл) кислорода, н.у.?
2. Из 3,85 г нитрата металла получено 1,6 г его гидроксида. Вычислите молярную массу эквивалентов металла.
1. Молярная масса кислорода, равная 32 г/моль, при н.у. занимает объем 22,4 дм3 (л), то объем молярной массы эквивалентов кислорода (8 г/моль) будет 22,4 : 4 = 5,6 л = 5600 мл.
По закону эквивалентов 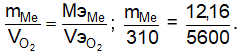
Отсюда = 310 · 12,16 : 5600 = 0,673 г.
Не нашел нужную задачу?