Решение задачи
1. Вычислить кажущуюся степень диссоциации хлористого водорода в ноль целых ноль две сотых нормальность растворе, если осмотическое давление равно 654 миллиметров ртутного столба при нормальной температуре
- Химия
Условие:
1. Вычислить кажущуюся степень диссоциации HCl в 0,02 н. растворе, если осмотическое давление равно 654 мм рт. ст. при нормальной температуре.
Решение:
Для диссоциирующих веществ осмотическое давление (в кПа) раствора определяется
по уравнению Вант-Гоффа с поправкой на диссоциацию электролита:
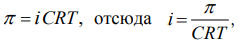 где i изотонический коэффициент; С молярная концентрация раствора .
где i изотонический коэффициент; С молярная концентрация раствора .
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
AI помощники
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э