Условие:
250 г раствора нитрата серебра подвергли электролизу при постоянной силе тока 1,93 А в течение некоторого времени. К полученному раствору добавили 80 г 2,0%-го раствора гидроксида натрия, щелочь прореагировала полностью. Выпавший осадок отфильтровали и высушили до постоянной массы, которая оказалась равна 1,16 г. Найдите массовую долю нитрата серебра в исходном растворе и время электролиза. Постоянная Фарадея F=96500 Кл/моль.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления ( указывайте единицы измерения и обозначения искомых физических величин).
Решение:
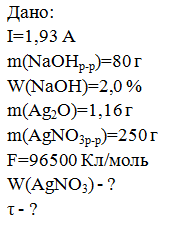
Рассмотрим процесс электролиза водного раствора нитрата серебра (І) с инертными электродами:
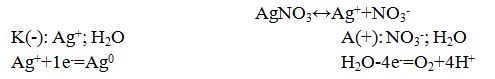
Суммарное уравнение электролиза:
