Условие:
Через водный раствор электролита пропустили ток силой I (ампер) в течение времени t часов. Выход по току принять 100 %.
- Напишите уравнение диссоциации электролита.
- Напишите уравнения процессов, протекающих на электродах при электролизе водного раствора электролита (анод инертный);
- Рассчитайте массы всех веществ, выделившихся на электродах.
- Если выделяются газообразные продукты, то рассчитайте их объемы.
Раствор электролита - Pb(NO3)2; I = 10,3 А; t = 1,2 ч.
Найти: т(Pb); V(О2) - ?
Решение:
1. Pb(NO3)2 Pb2+ + 2NO3-.
2. 0(Pb2+/Pb) = - 0,126 В.
В нейтральной среде 0(2Н+/Н20)рН=7 = - 0,412 В.
0(Pb2+/Pb) 0(2Н+/Н20)рН=7, поэтому на катоде выделяется свинец:
К: Pb2+ + 2е Pb0.
NO3- не окисляется в водном растворе, поэтому на аноде окисляются молекулы воды:
А: 2Н2О 4е О2 + 4Н+.
3. Массу свинца вычисляем по закону Фарадея:
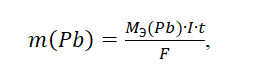
где т(Pb) масса свинца, выделившегося...
