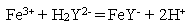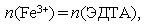Условие:
Для анализа отобрали 20,0 мл сточной воды, содержащей соединения железа, окислили их до Fe (III) и осадили в виде гидроксида. Промытый осадок растворили в HCl и оттитровали 4,05 мл 0,0505 М раствора ЭДТА. Вычислите массовую концентрацию (г/л) железа в сточной воде.