Для анализа взяли 10 см3 раствора NaOH, разбавили его в мерной колбе вместимостью 100 см3 дистиллированной водой до метки и хорошо перемешали. Затем отобрали 1 см3 приготовленного раствора и провели в присутствии фенолфталеина электролиз
- Химия
Условие:
Для анализа взяли 10 см3 раствора NaOH, разбавили его в мерной колбе вместимостью 100 см3 дистиллированной водой до метки и хорошо перемешали. Затем отобрали 1 см3 приготовленного раствора и провели в присутствии фенолфталеина электролиз при постоянной силе тока I = 10 мА, измеряя время электролиза. Провели 7 параллельных опытов. По данным таблицы 1 рассчитайте для каждого из 7 экспериментов молярную концентрацию эквивалента исходного основания и проведите их статистическую обработку.
Таблица 1
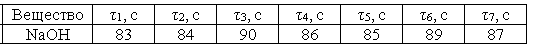
Решение:
В ходе электролиза водного раствора NaOH на аноде происходит химическая реакция
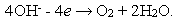
После того, как все ионы ОН- вступят в реакцию, среда станет нейтральной, фенолфталеин обесцветится.
Массу NaOH, вступившего в реакцию, можно вычислить по закону Фарадея:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства