Для металла выполните следующее: 1. Напишите электронную формулу. Укажите возможные степени окисления элемента. Определите ковалентность. Приведите примеры типичных соединений в данных степенях окисления (оксиды, гидроксиды, соли).
- Химия
Условие:
Для металла выполните следующее:
1. Напишите электронную формулу. Укажите возможные степени окисления элемента. Определите ковалентность. Приведите примеры типичных соединений в данных степенях окисления (оксиды, гидроксиды, соли).
2. Напишите уравнения реакций, характеризующих взаимодействие металла:
а) с простыми веществами (кислородом, серой, галогенами);
б) с растворами солей, оснований;
в) с разбавленной азотной кислотой;
г) с разбавленной соляной кислотой.
Возможность реакции в, протекающей в стандартных условиях, и реакции г, протекающей при парциальном давлении водорода P(H2) = 5×10–7 атм и концентрации HCl 0,01 моль/дм3, подтвердите расчетом.
3. Составьте уравнения реакций получения заданного металла в чистом виде из природного соединения или руды, используя один из промышленных методов (гидрометаллургический, металлотермический, пирометаллургический электрометаллургический, электрогидрометаллургический).
Металл — олово.
Решение:
1. Олово металл, расположенный в IVA-подгруппе 5 периода. Порядковый номер 50.
Электронная формула:
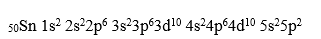
В данном состоянии два неспаренных электрона, ковалентность равна 2.
Для олова характерны степени окисления +2 и +4.
Примеры соединений:
SnO оксид олова (II)
Sn(OH)2 гидроксид олова (II)
SnCl2 хлорид олова (I)
SnO2 оксид олова (IV)
H2SnO3 оловянная кислота
SnCl4 хлорид олова (IV)
2. Химические сво...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства