Условие:
Для реакции 2HI(г) = H2(г) + I2(г) константа равновесия Kp = 1,83∙10–2 при 698,6 К. Сколько граммов HI образуется при нагревании до этой температуры 10 г I2 и 0,2 г H2 в трехлитровом сосуде? Чему равны парциальные давления H2, I2 и HI?
Решение:
Уравнение реакции:
2HI(г) = H2(г) + I2(г)
Kp = 1,83∙102
T = 698,6 К.
Вычисляем количества реагирующих веществ.
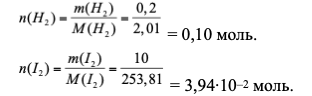
Пусть к моменту равновесия прореагировало моль I2. Из уравнения реакции следует, что прореагирует моль H2 и образуется 2 моль HI.
Равновесные количества составят:
[HI] = 2; [H2] = 0,10 ; [I2] = 3,94∙102 .
Всего в равновесной смеси: 2 + 0,10 + 3,94∙102 = 0,394 моль.
Равновесная мольная доля...
